Φτιάξτε μόνοι σας κρυστάλλους πρωτεΐνης Teach article
Μετάφραση από τον Αντώνη Γίτσα (Antonis Gitsas). Ο Beat Blattmann και ο Patrick Sticher από το Πανεπιστήμιο της Ζυρίχης (University of Zurich) στην Ελβετία, εξηγούν την επιστήμη πίσω από την…

είναι μικρά και εύθραυστα
αντικείμενα, με διάμετρο
μικρότερη από ένα χιλιοστό
και δύσκολο να
παρασκευαστούν. Παρόλα
αυτά είναι απαραίτητοι για
τις μελέτες δομικής
βιολογίας με ανάλυση
ακτίνων-Χ
Η εικόνα είναι ευγενική
προσφορά την Gaby
Sennhauser, University of
Zürich
Το 1959 ο Max Perutz και John Kendrew δημοσίευσαν ένα άρθρο για την τρισδιάστατη δομή της μυογλοβίνης φάλαινας, που είναι μια μικρή πρωτεΐνη υπεύθυνη για τη μεταφορά οξυγόνου στα κύτταρα της φάλαινας. Εξετάζοντας τη δομή της πρωτεΐνης, οι δυο ερευνητές ήθελαν να κατανοήσουν το μηχανισμό μεταφοράς οξυγόνου σε μοριακό επίπεδο. Έφτιαξαν κρυστάλλους αυτής της πρωτεΐνης και κατάφεραν να προσδιορίσουν τη δομή της αναλύοντας τη εικόνα περίθλασης ακτίνων-Χ από τον κρύσταλλο.
Στο παρελθόν μια σειρά μυογλοβίνης άλλων ειδών είχε μελετηθεί χωρίς μεγάλη επιτυχία, μέχρις ότου ο Perutz και ο Kendrew κατάφεραν να σχηματίσουν μια χρήσιμη εικόνα περίθλασης από κρυστάλλους μυογλοβίνης φάλαινας. Για αυτήν την πρωτοποριακή δουλειά τούς απονεμήθηκε το Βραβείο Νόμπελ Χημείας το 1962w1. Πενήντα χρόνια μετά πάντως, αποτελεί ακόμα πρόκληση η λήψη κρυστάλλων πρωτεΐνης για τη μελέτη της δομής.
Τι είναι οι πρωτεΐνες;
Οι πρωτεΐνες είναι η μεγαλύτερη ομάδα μη-υδατικών συστατικών των κυττάρων. Σχεδόν κάθε βιοχημική αντίδραση απαιτεί μια συγκεκριμένη πρωτεΐνη, που ονομάζεται ένζυμο. Άλλα είδη πρωτεϊνών έχουν μηχανικές και δομικές λειτουργίες (π.χ. το κολλαγόνο στον συνδετικό ιστό), ή διευθετούν την κυτταρική σηματοδότηση (π.χ. ορμονικοί υποδοχείς) τη ανοσολογική απόκριση (π.χ. αντισώματα) ή τη μεταφορά μικρών μορίων (π.χ. κανάλια ιόντων). Η γκάμα είναι τεράστια: Στον ανθρώπινο οργανισμό και μόνο είναι γνωστές περισσότερες από 20000 διαφορετικές πρωτεΐνες.
Παρόλη την ποικιλία τους, όλες οι πρωτεΐνες βασίζονται σε μια κοινή δομική αρχή: αποτελούνται από 20 διαφορετικά δομικά στοιχεία που λέγονται αμινοξέα, τα οποία διατάσσονται σε μια γραμμική αλυσίδα συνδεδεμένα με ομοιοπολικούς δεσμούς μεταξύ των αμινοξέων (βλέπε παρακάτω εικόνα). Το μήκος της πρωτεϊνικής αλυσίδας κυμαίνεται από μερικές δεκάδες μέχρι χιλιάδες αμινοξέων. Στα κύτταρα, κάθε πρωτεΐνη συντίθεται βάση των πληροφοριών που περιέχονται στο αντίστοιχο γονίδιο. Η σύνδεση γίνεται από ένα ριβόσωμα, που είναι μια πολύπλοκη μοριακή μηχανή αποτελούμενη από πρωτεΐνες και RNA.
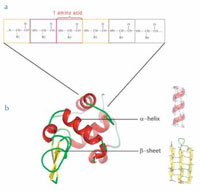
σχηματίζονται από
αμινοξέα που συνδέονται με
ομοιοπολικούς δεσμούς
σχηματίζοντας μια
γραμμική αλυσίδα
β. Οι πρωτεΐνες
αναδιπλώνονται σε μια
τρισδιάστατη δομή που
ορίζει τη λειτουργία τους.
Μικρά τμήματα της
αλυσίδας αμινοξέων
σχηματίζει αναδιπλώσεις.
Τα δύο κυριότερα δομικά
στοιχεία είναι οι α-έλικες
και τα β-φύλλα.
Κάντε κλικ στην εικόνα για μεγέθυνση
Η εικόνα είναι ευγενική
προσφορά τον Marc
Leibundgut, ETH Ζυρίχης, και
το www.pdb.org
Οι πρωτεΐνες αναδιπλώνονται σε διακριτές τρισδιάστατες δομές
Υπό κανονικές συνθήκες, οι γραμμικές αλυσίδες των αμινοξέων αναδιπλώνονται αυθόρμητα σε σαφείς τρισδιάστατες δομές. Οι σειρές των αμινοξέων σχηματίζουν χαρακτηριστικές δευτεροταγείς δομές. Οι πιο σημαντικές δομές είναι οι α-έλικες και τα β-φύλλα (βλέπε παρακάτω εικόνα), που σταθεροποιούνται από δεσμούς υδρογόνου μεταξύ αμινοξέων. Ολόκληρη η πρωτεΐνη σχηματίζει μια τριτοταγή δομή που αποτελείται από διάφορα τέτοια στοιχεία.
Η δομή είναι λειτουργικότητα: τι μας λέει η τρισδιάστατη δομή μιας πρωτεΐνης;
Η λειτουργία μια πρωτεΐνης εξαρτάται από την τρισδιάσταση δομή της. Μόνο όταν η πρωτεΐνη αναδιπλωθεί μπορούν συγκεκριμένα αμινοξέα της να είναι αρκετά κοντά μεταξύ τους ώστε να σχηματιστεί ένα ενεργό κέντρο. Αυτά τα κέντρα μπορούν να καταλύσουν βιοχημικές αντιδράσεις, όπως στην περίπτωση των ενζύμων, ή να σχηματίσουν ένα συγκεκριμένο σημείο σύνδεσης, όπως στην περίπτωση των αντισωμάτων. Η μελέτη των δομικών λεπτομερειών μιας πρωτεΐνης έχει μεγάλη σημασία για την κατανόηση του πώς λειτουργούν θεμελιώδεις διεργασίες της ζωής σε μοριακό επίπεδο: αυτό είναι το πεδίο έρευνας των δομικών βιολόγων. Μία από τις μεγαλύτερες προκλήσεις της δομικής βιολογίας σήμερα είναι η διασαφήνιση της δομής, της λειτουργίας και της αλληλεπίδρασης μεγάλων μακρομοριακών συμπλεγμάτων και πρωτεϊνών των μεμβρανώνw2. Λόγω της περιπλοκότητάς τους, αυτές οι πρωτεΐνες είναι ιδιαίτερα δύσκολο να μελετηθούν πειραματικά, και αποτελεί μεγάλο επίτευγμα κάθε φορά ο προσδιορισμός της δομής μιας τέτοιας πρωτεΐνης. Παρόλα αυτά, επειδή έχουν να κάνουν με θεμελιώδεις βιολογικές διεργασίες, το ενδιαφέρον για την καλύτερη κατανόηση της δομής και της λειτουργίας τους είναι αυξημένο, και οι επιστήμονες συνεχίσουν τις προσπάθειες για να πετύχουν την κρυστάλλωσή τους.
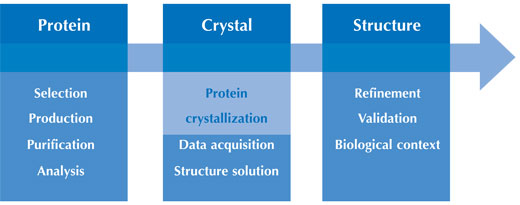
Η εικόνα είναι ευγενική προσφορά τους Beat Blattmann και Patrick Sticher
Οι πρωτεΐνες είναι πολύ μικρές για άμεση παρατήρηση
Οι πρωτεΐνες είναι μικροσκοπικές δομές, με διαστάσεις μόλις μερικών νανομέτρων (1 nm = 1 εκατομμυριοστό του mm). Αντικείμενα με τέτοιο μέγεθος δεν μπορούν να παρατηρηθούν ούτε καν με το ισχυρότερο οπτικό μικροσκόπιο, που έχει μέγιστη ανάλυση 1 μικρόμετρο (1 μm = 1 χιλιοστό του mm). Υπάρχουν κυρίως τρεις τεχνολογίες που κάνουν τις πρωτεΐνες “ορατές”:
- Περίθλαση ακτίνων-Χ από κρυστάλλους πρωτεϊνών
- Πυρηνικός μαγνητικός συντονισμός (NMR)
- Ηλεκτρονική κρυσταλλογραφία
Καθώς πάνω από το 90% όλων των πρωτεϊνικών δομών που καταχωρούνται στη δημόσια προσβάσιμη βάση δεδομένων βιολογικών μακρομορίωνw3 έχουν προσδιοριστεί με περίθλαση ακτίνων-Χ, θα εστιάσουμε σε αυτήν τη μέθοδο. Για να μάθετε περισσότερα για την ιστορία της κρυσταλλογραφίας και το ταξίδι μιας πρωτεΐνης από εργαστήριο σε εργαστήριο μέχρι να βρεθεί η δομή της, δείτε το άρθρο του Dominique Cornuéjols σε αυτό το τεύχος.
Η κρυστάλλωση των πρωτεϊνών είναι μια δύσκολη υπόθεση, επειδή είναι δύσκολο να προσδιοριστούν οι κατάλληλες συνθήκες υπό τις οποίες κάθε πρωτεΐνη κρυσταλλώνεται· μερικές φορές μοιάζει ακόμα και αδύνατο. Για να διασφαλιστεί λοιπόν σταθερή ποιότητα κρυστάλλων (δηλαδή ότι εξίσου καλοί κρύσταλλοι μπορούν να παραχθούν ξανά και ξανά), οι επιστήμονες χρησιμοποιούν ελεγχόμενες πειραματικές συνθήκες για να κρυσταλλώσουν τις πρωτεΐνες τους. Η πιο συνήθης μέθοδος στην κρυσταλλογραφία πρωτεϊνών είναι η μέθοδος διάχυσης ατμών (βλέπε εικόνα): με αυτή τη μέθοδο μια μικρή ποσότητα διαλύματος κρυστάλλωσης προστίθεται στο δοχείο του θαλάμου κρυστάλλωσης. Μια σταγόνα διαλύματος πρωτεΐνης και μια σταγόνα του διαλύματος κρυστάλλωσης αποτίθενται στην υπερυψωμένη θέση στο κέντρο του θαλάμου.
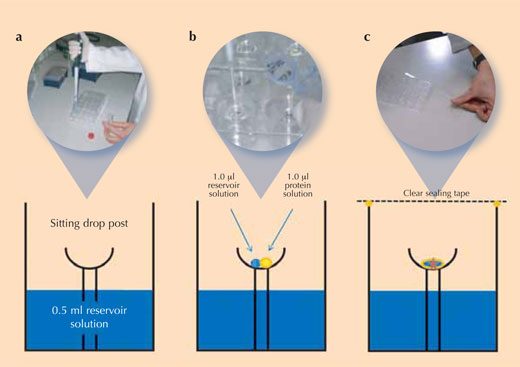
Η εικόνα είναι ευγενική προσφορά τους Beat Blattmann και Patrick Sticher
Αμέσως αφότου προσθέσουμε όλα τα διαλύματα ο θάλαμος σφραγίζεται για να εμποδιστεί η εξάτμιση. Επειδή η συγκέντρωση των ιόντων άλατος είναι μεγαλύτερη στο διάλυμα κρυστάλλωσης από το μίγμα στο υπερυψωμένο στήριγμα, μόρια διαλύτη θα κινηθούν από τη σταγόνα της πρωτεΐνης προς το δοχείο με διάχυση ατμών στην αέρια φάση. Κατά τη διάρκεια αυτής της διαδικασίας η διαλυτότητα της πρωτεΐνης στη σταγόνα ελαττώνεται. Το διάλυμα της πρωτεΐνης στη σταγόνα τελικά γίνεται υπερκορεσμένο, μια κατάσταση που είναι θερμοδυναμικά ασταθής. Αυτό έχει ως αποτέλεσμα μέρος της πρωτεΐνης στη σταγόνα είτε να σχηματίσει κρυσταλλικούς πυρήνες που τελικά θα μεγαλώσουν για να γίνουν μεγάλοι κρύσταλλοι πρωτεΐνης (βλέπε εικόνα), είτε να ιζηματοποιηθεί ως άμορφη πρωτεΐνη, άχρηστη για ανάλυση με ακτίνες-Χ. Η κρυστάλλωση και η ιζηματοποίηση είναι ανταγωνιστικές διεργασίες, και γι’ αυτό είναι εξαιρετικά σημαντικό να βρεθούν οι κατάλληλες συνθήκες που ευνοούν την κρυστάλλωση.
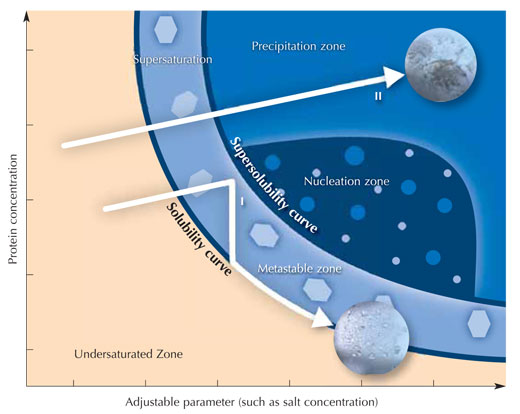
Η εικόνα είναι ευγενική προσφορά την Nicola Graf
Κρύσταλλοι λυσοζύμης στην τάξη
Σε αυτήν τη δραστηριότητα οι μαθητές θα μάθουν περισσότερα για τη σύγχρονη κρυσταλλογραφία ακτίνων-Χ προσδιορίζοντας τις ιδανικές συνθήκες κρυστάλλωσης μιας πρωτεΐνης. Μελετούν το σχηματισμό κρυστάλλων λυσοζύμης ως συνάρτηση του pH και της συγκέντρωσης άλατος.
Λυσοζύμη
Η λυσοζύμη είναι μια πρωτεΐνη που ανήκει στην οικογένεια των αντιβακτηριακών ενζύμων, η οποία καταστρέφει τα κυτταρικά τοιχώματα των βακτηρίων. Στους ανθρώπους βρίσκεται σε αφθονία σε μια σειρά εκκρίσεων, όπως τα δάκρυα, το σάλιο, και η βλέννα.
Εξοπλισμός και υλικά
- Ένας ή δύο δίσκοι κρυστάλλωσης Cryschem™ (Hampton Research) ανά τάξη
- Διάφανη μονωτική ταινία (5 cm) (Hampton Research)
- Χειροκίνητες πιπέτες 1 ml και 1 μl
- Ένα μικροσκόπιο για την παρατήρηση των κρυστάλλων
- Αποθηκευτικός χώρος στους 20 °C
Χημικά
- Λυσοζύμη (SigmaAldrich αριθμός προϊόντος 62971, BioChemika grade – λυσοζύμη από διαφορετική πηγή είναι επίσης κατάλληλη, αλλά η συγκεκριμένη έχει ελεγχθεί εκτενώς με αυτό το πρωτόκολλο, και γι’ αυτό συνιστάται ώστε να είστε σίγουροι)
- Χλωριούχο νάτριο (NaCl) (μαγειρικό αλάτι από το σούπερ μάρκετ είναι μια χαρά)
- Κιτρικό οξύ
- Οξικό νάτριο
- Μονοβασικό φωσφορικό νάτριο
- Αραιωμένο διάλυμα υδροξειδίου του νατρίου
- Άνυδρο αιθανικό οξύ
- Απιονισμένο νερό
Ρυθμιστικά διαλύματα
Τα παρακάτω υδατικά ρυθμιστικά διαλύματα θα πρέπει να ετοιμαστούν από τον διδάσκοντα εκ των προτέρων:
- Υδατικό διάλυμα λυσοζύμης 50 mg/ml
- 3 M χλωριούχο νάτριο
Διαλύστε 17.53 g NaCl σε 100 ml απιονισμένο νερό. - 1 M κιτρικό νάτριο, pH 3.5
Διαλύστε 19.24 g κιτρικού οξέος σε in 100 ml απιονισμένο νερό. Ρυθμίστε το pH στο 3.5 με το διάλυμα υδροξειδίου του νατρίου. - 1 M οξικό νάτριο, pH 4.5
Διαλύστε 13.6 g οξικού νατρίου σε 100 ml απιονισμένο νερό. Ρυθμίστε το pH στο 4 με άνυδρο αιθανικό οξύ. - 1 M οξικό νάτριο, pH 5.5
Διαλύστε 13.6 g οξικού νατρίου σε 100 ml απιονισμένο νερό. Ρυθμίστε το pH σε 5.5 με άνυδρο αιθανικό οξύ - 1 M φωσφορικό νάτριο, pH 6.5
Διαλύστε 15.6 g φωσφορικό νάτριο σε 100 ml απιονισμένο νερό. Ρυθμίστε το pH σε 6.5 με το διάλυμα υδροξειδίου του νατρίου.
Πείραμα ανάπτυξης κρυστάλλων
- Από τα ρυθμιστικά διαλύματα ετοιμάστε τα 24 διαλύματα δοχείου (reservoir στην εικόνα 4) για τα πειράματα κρυστάλλωσης σύμφωνα με τον πίνακα. Οι μαθητές μπορούν να χωριστούν σε μικρές ομάδες, η κάθε μία από τις οποίες θα ετοιμάσει μερικά από τα 24 διαφορετικά διαλύματα. Όλες οι ομάδες μπορούν να χρησιμοποιήσουν τα ίδια ρυθμιστικά διαλύματα.
- Χρησιμοποιώντας τον πίνακα ως αναφορά, βάλτε με την πιπέτα 0.5 ml του αντίστοιχου διαλύματος δοχείου σε ένα από τα αντίστοιχα 24 δοχεία ενός δίσκου Cryschem™ ((‘a’ στην παραπάνω εικόνα). Στον πίνακα συνοψίζονται οι συνθήκες κάθε δοχείου και η θέση τους στο δίσκο.
- Μεταφέρετε με την πιπέτα 1 μl του διαλύματος δοχείου στην υπερυψωμένη θέση κάθε δοχείου (‘b’ στην παραπάνω εικόνα).
- Συγκρίνοντας τα αποτελέσματα από τα 24 δοχεία, προσδιορίστε τις βέλτιστες συνθήκες κρυστάλλωσης.
- Αναλύστε το μέγεθος, το πλήθος και την κατανομή των κρυστάλλων λυσοζύμης. Οι κρύσταλλοι ίσως είναι πολύ μικροί για να είναι ορατοί με γυμνό μάτι, επομένως ένας μεγεθυντικός φακός ή – ακόμα καλύτερα – ένα μικροσκόπιο είναι πολύ χρήσιμα.
- Διατηρήστε το δίσκο στους 20 °C. Οι κρύσταλλοι θα αρχίσουν να αναπτύσσονται αμέσως σε μερικά δοχεία, και η ανάπτυξη μπορεί να παρατηρηθεί απευθείας με μικροσκόπιο ανά 1-2 ώρες. Οι δίσκοι μπορούν να φυλαχθούν μέχρι το επόμενο μάθημα για την τελική ανάλυση. Μετά από 1-2 εβδομάδες, οι κρύσταλλοι θα έχουν το τελικό τους μέγεθος. Ένας σφραγισμένος δίσκος διατηρείται για ένα χρόνο ή και παραπάνω.
- Αμέσως αφού προσθέσετε τις σταγόνες του διαλύματος πρωτεΐνης, κλείστε το σκεύος κρυστάλλωσης με διάφανη μονωτική ταινία ώστε να μην εξατμιστούν τα διαλύματα (‘c’ στην παραπάνω εικόνα).
- Προσθέστε 1 μl ρυθμιστικού διαλύματος λυσοζύμης για κάθε 1 μl ρυθμιστικού διαλύματος (‘b’ στην παραπάνω εικόνα).
| 1 | 2 | 3 | 4 | 5 | 6 | ||
|---|---|---|---|---|---|---|---|
| 2.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 0.6 M) σε 7.0 ml απ. νερό | 3.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 0.9 M) σε 6.0 ml απ. νερό | 4.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 1.2 M) σε 5.0 ml απ. νερό | 5.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 1.5 M) σε 4.0 ml απ. νερό | 6.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 1.8 M) σε 3.0 ml απ. νερό | 7.0 ml ρυθμιστικό διάλυμα 3M NaCl (τελική συγκέντρωση 2.1 M) σε 2.0 ml απ. νερό | ||
| A | 1.0 ml κιτρικό νάτριο (τελική συγκέντρωση 0.1 M), pH 3.5 | A1 | A2 | A3 | A4 | A5 | A6 |
| B | 1.0 ml οξικό νάτριο (τελική συγκέντρωση 0.1 M), pH 4.5 | B1 | B2 | B3 | B4 | B5 | B6 |
| C | 1.0 ml οξικό νάτριο (τελική συγκέντρωση 0.1 M), pH 5.5 | C1 | C2 | C3 | C4 | C5 | C6 |
| D | 1.0 ml φωσφορικό νάτριο (τελική συγκέντρωση 0.1 M), pH 6.5 | D1 | D2 | D3 | D4 | D5 | D6 |
Μελετήστε τους κρυστάλλους σας με ακτίνες-Χ
Όταν η τάξη σας ετοιμάσει επιτυχώς κρυστάλλους πρωτεΐνης, παρακαλούμε επικοινωνήστε με τον Dr Patrick Sticher στο sticher@bioc.uzh.ch. Το ελβετικό NCCR (National Center of Competence in Research) Structural Biologyw2 προσφέρθηκε να παρέχει μια εικόνα περίθλασης ακτίνων-Χ στις πρώτες 10 τάξεις που θα ετοιμάσουν κρυστάλλους πρωτεΐνης χρησιμοποιώντας αυτό το πρωτόκολλο. Οι μετρήσεις ακτίνων-Χ μπορούν να γίνουν είτε απευθείας με τα σχολικά δείγματα, είτε – αν είναι αδύνατη η αποστολή τους – αναπαράγοντας τις ιδανικές συνθήκες κρυστάλλωσης που βρήκε η τάξη σας και μετρώντας τα νέα δείγματα. Μαζί με την εικόνα περίθλασης οι επιστήμονες μπορούν να σας στείλουν επιπλέον πληροφορίες σχετικά με το τι θα έκαναν στη συνέχεια με αυτά τα δεδομένα για να βρουν την ακριβή δομή, καθώς και ένα πιστοποιητικό αν θέλετε.
Μιλήστε με τους επιστήμονες
Οι μαθητές μπορούνε να συνομιλήσουν online με τους επιστήμονες μέσω του Skypew4, αφού εκτελέσουν τα δικά τους πειράματα. Για να κλείσετε ένα ραντεβού, στείλτε ένα e-mail στον Patrick Sticher (sticher@bioc.uzh.ch) για να μιλήσετε μαζί του μέσω του λογαριασμού Skype ‘proteincrystallography’.
Κατεβάστε επιπλέον διδακτικό υλικό
Μια σειρά διαφανειών Powerpoint, εικόνων, και περαιτέρω πειραμάτων παρέχονται onlinew5.
Προμηθευτές
Οι παρακάτω προμηθευτέςw6 παρέχουν τα απαραίτητα υλικά και χημικά προϊόντα:
Hampton Research:
- Cryschem™ 24-1 SBS plate, Cat. No. HR1-002 (Συνιστούμε να χρησιμοποιήσετε αυτόν τον τύπο δίσκου. Ένας δίσκος κοστίζει περίπου 3 $.)
- Crystal Clear Sealing Tape (5 cm), Cat. No. HR4-51
Gilson Inc:
- 1 ml και 1 μl manual pipettes
Sigma Aldrich:
- Lysozyme, αριθμός προϊόντος 62971
- Sodium chloride, αριθμός προϊόντος 71380
- Citric acid, αριθμός προϊόντος 27488
- Sodium acetate, αριθμός προϊόντος 71190
- Sodium phosphate, monobasic, αριθμός προϊόντος 71502
References
- Cornuéjols D (2009) Biological crystals: at the interface between physics, chemistry and biology. Science in School 11: 70-76. www.scienceinschool.org/2009/issue11/crystallography
Web References
- w1 – Επιπλέον πληροφορίες για τους βραβευθέντες με βραβείο Νόμπελ στη χημεία το 1962 και την πρωτοποριακή τους δουλειά μπορούν να βρεθούν στον ιστότοπο της Επιτροπής του Βραβείου Νόμπελ: http://nobelprize.org/nobel_prizes/chemistry/laureates/1962
- w2 – Το ελβετικό National Center of Competence in Research (NCCR) είναι μια κοινοπραξία επιστημόνων αφοσιωμένων στην κατανόηση των σχέσεων δομής-λειτουργίας των πρωτεϊνών των μεμβρανών και υπερμοριακών συμπλεγμάτων: www.structuralbiology.uzh.ch
-
Επιλεγμένες ερευνητικές μελέτες μπορούν να βρεθούν εδώ:www.structuralbiology.uzh.ch/research004.asp
-
- w3 – Νέες δομές βιολογικών μακρομορίων (πρωτεΐνες και νουκλεικά οξέα) καταχωρούνται στη βάση δεδομένων Protein DataBank (PDB). Ο ιστότοπος παρέχει μια πληθώρα από ενδιαφέρουσες διδακτικές πηγές: www.pdb.org
-
Ακόμα μία χρήσιμη πηγή για πληροφορίες σχετικά με τις πρωτεΐνες είναι η εξής:: www.proteopedia.org
-
- w4 – Για να κατεβάσετε και να εγκαταστήσετε το Skype, δείτε: www.skype.com
- w5 – Επιπλέον διδακτικές πηγές διατίθενται εδώ: www.structuralbiology.uzh.ch/teacher
-
Όνομα χρήστη: crystallization
-
Κωδικός: xraybeam2008
-
Ο ιστότοπος θα ενημερώνεται τακτικά.
-
- w6 – Οι ιστότοποι των προμηθευτών είναι οι εξής:
-
Hampton Research: www.Hamptonresearch.com
-
Gilson Inc.: www.gilson.com
-
Sigma-Aldrich: www.sigmaaldrich.com
-
Resources
- Abad-Zapatero C (2002) Crystals and Life: A Personal Journey. La Jolla, CA, USA: International University Line. ISBN: 978-0972077408
- Να μερικά συνιστώμενα πρωτόκολλα για την ανάπτυξη μη-πρωτεϊνικών κρυστάλλων με νεότερους μαθητές:
Review
Το άρθρο αυτό παρέχει μια καλή εισαγωγή στη μελέτη πρωτεϊνών με περίθλαση ακτίνων-Χ. Έτσι παρέχει μια ενδιαφέρουσα και ολοκληρωμένη άσκηση για το μάθημα της βιολογίας, τη χημείας και τη φυσικής, διασυνδέοντας τις τρεις επιστήμες. Μπορεί να χρησιμοποιηθεί για να συζητηθεί πώς μελετούμε τη μικροσκοπική κλίμακα και γιατί είναι απαραίτητο να εξετάζουμε τα πράγματα σε αυτό το επίπεδο. Το άρθρο προσφέρεται ως ανάγνωσμα για ένα καλό υπόβαθρο για διδάσκοντες που δεν είναι εξοικειωμένοι με τη χρήση της περίθλασης ως αναλυτικού εργαλείου.
Το πρακτικό μέρος αναμένεται να χρειαστεί κάποιο χρόνο μέχρι την προετοιμασία και τη λήψη αποτελεσμάτων, αλλά η δυνατότητα ανάλυσης των αποτελεσμάτων σε ένα πανεπιστήμιο δίνει άλλη διάσταση στην πρακτική εξάσκηση.
Mark Robertson, Ηνωμένο Βασίλειο





