Neutrons i anticongelant: investigant els peixos de l’Àrtic Understand article
Traduït per Rosa Codolà. Matthew Blakeley de l’ ILL i els seus companys de l’ ESRF entre d’altres han descobert l’anticongelant en la sang dels peixos de l’Àrtic que els manté vius a temperatures sota zero. Ell i Eleanor Hayes ens ho expliquen.

(Myoxocephalus scorpius)
també té proteïnes
anticongelants
Imatge de domini públic;
origen de la imatge: Wikimedia
Commons
Quan pensem en l’Àrtic, molts de nosaltres pensem en icebergs, óssos polars i foques. Temperatures de congelació, vents gelats i desolats erms nevats – un repte per a qualsevol animal que hi visqui.

àrtiques han obligat els
animals a desenvolupar
algunes adaptacions
sorprenents.
Imatge cortesia de ucumari;
origen de la imatge: Flickr
Estem familiaritzats amb moltes de les formes amb les que els animals de l’Àrtic s’han adaptat al seu entorn: l’espessa pell dels óssos polars, la gruixuda capa de greix de les foques, els hàbits migratoris d’algunes aus. Aquests animals, però, són endoterms – mantenen una temperatura corporal constant, molt per sobre de la del seu gelat entorn.
Per els peixos, la situació és molt diferent – la majoria són exotèrmics, el que significa que els seus cossos tenen la mateixa temperatura que el seu entorn. I els seus voltants són realment molt freds: l’oceà Àrtic arriba amb freqüència a temperatures tan baixes com -1 ° C, només l’alt contingut en sal de l’aigua impedeix que es congeli.
La sang dels peixos, bastant menys salada que l’oceà, podria congelar-se a -0.5ºC. Per evitar això, els peixos de l’Àrtic han desenvolupat proteïnes especialitzades amb propietats anticongelants (AFPs, antifreeze proteins).

origen de la imatge: Flickr
Les AFPs tenen una tasca complexa. Per evitar que el peix es mori per congelació, han d’unir-se als nuclis de cristal·lització del gel que es formen en el cos del peix i així evitar que els cristalls de gel creixin. Però, com diferencia l’AFP el cristall de gel de l’aigua líquida?
Les AFP han sigut exahustivament estudiades amb diferents tècniques, com la difracció de raigs X, revelant l’existència d’una superfície especialitzada en unir-se al gel.
La difracció de raigs X es basa en la dispersió (difracció) d’aquests rajos produïda pel núvol d’electrons que envolta cada àtom. Les molècules tenen patrons de difracció característics. Tanmateix, els àtoms d’hidrogen (i els de deuteri), que tenen un sol electró, dispersen els raigs X molt poc (Figura 1a, a continuació), de manera que la senyal de difracció de raigs X per a l’aigua (H2O) és molt semblant a la dels àtoms d’oxigen (O). Com a resultat, quan els científics van tractar d’examinar com interactuava la superfície d’unió amb el gel i el gel, no van ser capaços d’identificar totes les molècules d’aigua de la superfície.
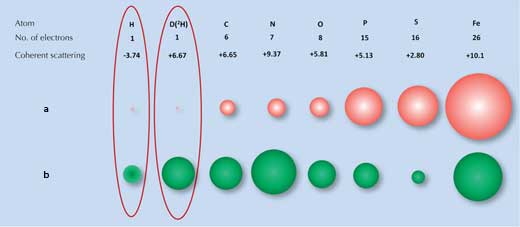
a) Els electrons dispersen els raigs X, la força de la dispersió (mida de les rodones vermelles) és proporcional al nombre d’electrons.
b) Els nuclis dispersen els neutrons, la força de la dispersió (mida de les rodones de color verd) depèn de forces específiques de cada nucli
Imatge cortesia de Matthew Blakeley

proteïnes anticongelants del
peix Zoarces americanus.
Imatge cortesia de Derek
Keats; origen de la imatge:
Flickr
Aquí és on una segona tècnica, la difracció de neutrons, és útil. Els neutrons es veuen dispersats pels nuclis atòmics i no pels d’electrons, a més la intensitat de la dispersió depèn de forces nuclears específiques. Aquestes forces, són diferents per cada element, i també pels seus diferents isòtops, ja que el nombre de neutrons en el seu nucli és diferent (Figura 1b, dalt). Per sort per a nosaltres, els àtoms d’hidrogen poden ser detectats fàcilment utilitzant la dispersió de neutrons i el deuteri (isòtop pesat de l’hidrogen, que té un neutró extra) també pot detectar-se amb més fiabilitat. Per tant el senyal obtingut a partir de l’aigua serà significativament diferent del de l’oxigen.
Nosaltres (Matthew Blakeley i els seus col·laboradors científics) varem decidir investigar un tipus d’AFP de la sang del peix de l’Àrtic: en concret la AFP de tipus III. Per evitar els problemes que van tenir altres investigadors, vam utilitzar una combinació de raigs X i difracció de neutrons a fi d’examinar l’estructura de les proteïnes i les seves interaccions amb les molècules d’aigua. Hem realitzat els nostres experiments a les instal·lacions de l’Institut Laue-Langevin (ILL)w1 i la Instal·lació Europea de Radiació Sincrotró (European Synchrotron Radiation Facility, ESRFw2; veure quadre, inferior). La investigació amb neutrons d’uns cristalls tan petits ha estat possible gràcies als avenços dels últims anys de l’ILL pel que fa a la preparació de la mostra i a l’instrumental emprat.
Com és habitual en les investigacions d’estructures de proteïnes, s’insereix el gen sintètic per a la AFP de tipus III en Escherichia coli, es sobre-expressa el gen de manera que ens permeti recollir suficient quantitat de proteïna. Es suministra aigua pesada (que conté deuteri en lloc d’àtoms normals d’hidrogen) als bacteris, per assegurar-se que la proteïna resultant era perdeuterada (subtitució dels àtoms d’hidrogen per deuteri). A continuació, van cristal·litzar la proteïna per ppoder determinar la seva estructura, comprovant que la forma de la proteina perdeuterada tenia la mateixa estructura que la forma normal. (Veure Cornuéjols, 2009, i Blattmann & Sticher, 2009, per aprofundir en la cristal·lografia de proteïnes i fins i tot fer una cristal·lització tu mateix.)
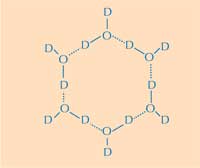
per sis molècules d’aigua. D
= deuteri; O = oxigen. Fer clic
sobre la imatge per
ampliar-la
Imatge cortesia de Nicola Graf
Part de la resposta de com les AFP de tipus III poden diferenciar el gel de l’aigua en estat líquid es troba en la diferent estructura de les AFP comparada amb les proteïnes típiques, aquestes últimes normalment tenen aminoàcids hidrofòbics situats cap el centre de la seva estructura (allunyats de les molècules d’aigua del seu entorn) i aminoàcids hidròfils en la seva superfície. Com han demostrat altres investigadors, les AFP són especials pel fet de tenir molts aminoàcids hidrofòbics en la seva superfície, impedint que la proteïna s’uneixi a l’aigua líquida mitjançant ponts d’hidrogen. Aquests aminoàcids hidrofòbics superficials s’uneixen als nuclis de cristal·lització del gel, però no a l’aigua líquida. Com funciona això?
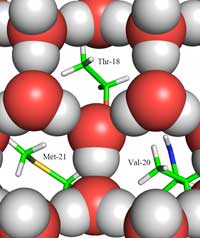
gel (que es mostra amb boles
vermelles i grises) i el lloc
d’unió proteïna- gel, mostra
els grups metil dels residus
hidrofòbics Thr-18, Val i
Met-20-21, orientats cap els
forats de l’anell de gel. Fer
clic sobre la imatge per
ampliar-la
Copyright © 2011 John Wiley &
Sons, Ltd; origen de la imatge:
Howard et al. (2011)
Aquí està la segona part de la resposta: en què difereix l’estructura del glaç de la de l’aigua líquida. Utilitzant la difracció de neutrons, podem localitzar les posicions de les molècules d’aigua sobre la superfície proteica d’unió amb el gel. Hem identificat un grup tetraèdric de molècules d’aigua unides a la superfície de la proteïna en el punt d’unió amb el gel. Aquest grup tetraèdric es troba com aigua en estat líquid (com en el nostre experiment), però també és típic del gel, aquesta dada ens va donar el punt d’inici per modelar la resta del cristall de gel i deduir la forma en que s’uneixen a la AFP. El model resultant està format per anells de sis molècules d’aigua en el que es coneix com a configuració en vaixell: sis molècules d’aigua en disposició hexagonal, deixant un forat al mig (vegeu la Figura 2, a dalt). Aquest és el forat que permet a les AFP de tipus III distingir l’estructura dels nuclis de gel de la de l’aigua: les regions hidrofòbiques de la proteïna encaixen en els forats, la unió es fa a través de forces de Van der Waals (Figura 3). Per contra, l’aigua líquida no té cap forat on les regions hidrofòbiques, com els grups metil puguin unir-se. Això impedeix el contacte entre l’aigua líquida i la superfície de proteïna, factor necessari per crear una interacció més estreta.

de l’Àrtic si no tinguessin
proteïnes anticongelants?
Imatge cortesia de
dwleindecker / iStockphoto
Encara que altres investigadors han proposat que els residus hidrofòbics juguen un paper important en com les AFPs de tipus III reconeixen els cristalls del nuclis de gel, ens trobem amb les primeres dades experimentals que ho corroboren.
És interessant aprendre més sobre com els peixos de l’Àrtic poden sobreviure en el seu ambient, però a més aquesta recerca també té possibles aplicacions industrials. Les AFPs de tipus III han estat incorporades a un gelat per minimitzar la formació de grans cristalls de gel i millorar així la seva consistència. En el futur, els gens codificadors de les AFPs poden ser incorporats als cultius perquè puguin créixer en ambients sota zero.
Més informació sobre ILL i ESRF

L’ Institut Laue-Langevin (ILL)w1 és un centre internacional d’investigació a l’avantguarda de la ciència i la tecnologia de neutrons. Opera una de les fonts de neutrons més intensa del món, subministrant feixos de neutrons per a un conjunt de 40 instruments d’alt rendiment que estan en continua actualització.
Com a centre de suport a la investigació, ILL posa les seves instal·lacions i coneixements a disposició dels científics visitants. Cada any, uns 1.200 investigadors de més de 30 països visiten ILL de Grenoble, França. Més de 800 experiments es duen a terme cada any, centrats principalment en ciència bàsica en una varietat de camps: física de lamatèria condensada, química, biologia, física nuclear i ciència dels materials.
La Instal·lació Europea de Radiació Sincrotró (European Synchrotron Radiation Facility, ESRF)w2 és un centre d’investigació internacional, compartint emplaçament amb ILL de Grenoble, França. Emet feixos de raigs X d’alta brillantor, que són utilitzats, cada any, per milers de científics de tot el món.
La complementarietat entre els raigs X emesos pel sincrotró i els feixos de neutrons pot ajudar-nos a entendre com funcionen sistemes complexos, com ara les AFPs com s’explica en aquest article. Per aprofitar al màxim la sinergia entre sincrotró i neutró, ESRF i ILL han sigut decisius en la creació de l’Associació per la Biologia Estructural (Partnership for Structural Biology, PSB) i l’Associació per a la Matèria Condensada (Partnership for Soft-Condensed Matter), són d’esperar altres associacions en un futur pròxim.
ILL i ESRF són membres de EIROforumw3, que publica Science in School.
References
- Blattmann B, Sticher P (2009) Growing crystals from protein. Science in School 11: 30-36.
- Cornuéjols D (2009) Biological crystals: at the interface between physics, chemistry and biology. Science in School 11: 70-76.
- Howard EI, Blakeley MP et al. (2011) Neutron structure of type-III antifreeze protein allows the reconstruction of AFP–ice interface. Journal of Molecular Recognition 24: 724-732. doi: 10.1002/jmr.1130
Web References
- w1 – Per saber més d’ ILL, consultar: www.ill.eu
- w2 – Per saber més d’ ESRF i PSB, consultar www.esrf.eu i www.psb-grenoble.eu
- w3 – Per més detalls d’ EIROforum, consultar: www.eiroforum.org
Institutions
Review
Si alguna vegada t’has preguntat com poden sobreviure els peixos en els oceans gelats, pots trobar la resposta en aquest interessantíssim article, que porta el lector a través d’una investigació científica sobre l’estructura de les proteïnes i les seves interaccions.
L’article pot ser utilitzat com a lectura de fons en l’estudi de biomolècules o com a base d’una discussió sobre el paper de les proteïnes en els organismes vius. Algunes preguntes per avaluar la comprensió de l’article:
- Descriu l’adaptació dels peixos a les gelades aigües àrtiques
- Com actuen les proteïnes AFPs d’anticongelant en la sang del peix?
- Quines són les limitacions de la difracció de raigs X a l’estudiar les AFPs?
- En què difereixen les difraccions de neutrons de les de raigs X?
- Descriu pas a pas el camí per identificar l’estructura de les AFPs
- En què difereixen les AFPs d’altres proteïnes?
- Com distingeixen les AFPs l’aigua en estat gel de les molècules d’aigua líquida?
Angela Charles, Malta





