Нов поглед към светлината: построй си спектрометър Teach article
Превод Бойко Григоров (Bojko Grigorov). Вземи едно CD и една бисквитена кутия, и какво имаш? С малко помощ от Марк Тиеле Вестра- твой собствен спектрометър! Време e да…
Astronomy Observatory/
Association of Universities
for Research in Astronomy/
National Science Foundation
Бялата светлина всъщност не е бяла – тя се състои от много различни цветове. Състава на светлината – нейния спектър – се изучава с помоща на инструмент наречен спектрометър. В тази статия, ние разкриваме как можете да си построите напълно функциониращ спектрометър с помоща на компакт диск и бисквитена кутия. Ние ще използваме този “Направи си сам” инструмент за да се наслаждаваме на чудесния свят на скритите цветове зад най-обикновенни всекидневни предмети като електрически крушки, флуоресцентни лампи, компютърни монитори и свещи!
Да започнем!
Как да разделим светлината?
Има няколко начина да се разцепи бялата светлина на съставящите я различни цветове. Един от начините е да се използва призма, както Нютон е направил. Благодарение на вариациите в рефракционния индекс, различните цветове следват различен път през призмата, което е причина за разделянето им.

повърхността на компакт
диск
Снимка от Марк Тиеле Вестра
Друг начин е т.н. дифракционна решетка, която се състои от голям брой миниатюрни бразди, паралелни една на друга, както е показано на снимката долу.
Интеракцията на тези бразди със светлинните вълни води до отразяване на различните цветове в различни посоки.
За щастие всеки има у дома висококачествена дифракционна решетка: Компакт диск (CDs). Прекрасните цветове които се виждат когато светлината рефлектира от повърхността на CD-то са ясна индикация че той действа като дифракционна решетка. Но защо? Илюстрацията по-горе показва как едно силно увеличение на повърхността на CD би изглеждало. Музиката е кодирана като кратки и дълги канали, които са разположени в един дълъг спирален канал на повърхността на CD. Тези канали, които са разположени само на 1.6µm (1600 nm) един от друг, действат като решетка.
Конструиране на спектрографа
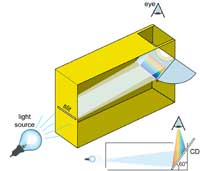
спектрометъра. CD се
разполага под ъгъл от 600
спрямо дъното на кутията
Снимка от Марк Тиеле Вестра
Можем да използваме тази домашна дифракционна решетка за конструиране на нашия спектрометър. Той се състои от два важни елемента: едно CD, което разделя светлината на различните съставящи я цветове, и тесен процеп на противната страна на кутията който продуцира тесен лъч светлина.
Процепа е на едната страна на кутията, направен с помоща на дебела хартия и скоч. Малко по-луксозен модел може да се направи от две бръснарски ножчета, които се залепват със скоч едно срещу друго, както е показано на снимката. Ако процепа е много широк, спектъра ще бъде малко замъглен, но ако е много тесен, спектъра ще бъде тъмен. Широчина от 0.2 мм изглежда най-добре, но вие може да експериментирате. Качеството на спектъра е зависим от качеството на процепа, така че трябва да се направи много внимателно.
На другата страна на кутията, едно CD (авторът е използвал празно CD) е монтирано под ъгъл 600 на дъното на кутията. Отгоре има дупка през която може да се наблюдава CD-то. Разсеяна светлина се изолира като се покрият всички дупки и процепи с черно тиксо.
За да се наблюдава спектъра, процепа е разположен срещу източник на светлина (колкото по-близко по-добре), и наблюдателя гледа през дупката отгоре. Движи кутията леко да добиеш чувство на какво да обърнеш внимание. Снимки могат да се направят с проста дигитална камера, с макро за предпочитане, закрепена с тиксо или гумена лента. Добре би било да е камера с мануален фокус, тъй като би било трудно да се направи добра снимка на ауто-фокус.
Наблюдения

Снимка от Марк Тиеле Вестра

Снимка от Марк Тиеле Вестра
Време за екперименти! Първият опит е да се наблюдава спектъра на обикновенна електрическа крушка. Резултата е показан по-долу.
Виждаме една хубав, непрекъснат спектър, с всички цветове на дъгата. В този вид лампи светлината се продуцира от много гореща метална жичка.
След това ние поглеждаме към две различни флуоресцентни лампи, които излъчват бяла светлина.
Първата, която е обикновенна флуоресцентна лампа, показва няколко отчетливи линии на фона на непрекъснат спектър. Тези емисионни линии(виж текста по-долу) са продуцирани от живачни изпарения с ниска концентрация. Живакът продуцира също така ултравиолетова светлина, която се превръща в непрекъснат спектър от видима светлина посредством тънък слой от фосфор намазан от вътрешната страна на тръбата.
Втората флуоресцентна лампа (виж по-долу) показва много различен спектър. Причината е че производителят може да варира цвета на светлината като използва различни комбинации от фосфор. Илюстрираната лампа използва фосфор който емитира непрекъснат спектър, но този тип използва т.н. трицветен фосфор: комбинация от три типа фосфор всеки от който има свой комплект от емисионни линии. Ние виждаме смесицата от цветове като бяла.
Една малка част от екрана на лаптопа показваща бял документ продуцира спектъра показан долу. Триточковите цветове които образуват този имидж – червен, зелен и син – са ясно очертани.

Снимка от Марк Тиеле Вестра

Снимка от Марк Тиеле Вестра
Как се формират спектрите
Някои от спектрите които се виждат с помоща на нашия спектрометър имат непрекъснат фон, като цветовете варират меко с преход от тъмно червен до тъмно син. Други се състоят от резки линии на непрекъснат фон, резки линии без фон, или даже тъмни линии на непрекъснат фон, подобно на слънчевия спектър (виж долу). Защо е цялото това разнообразие? Как се формират спектрите?
Дължи се на атомите. Индивидуален атом може да се намери в различни енергийни състояния, зависещи от електроните им и техното орбитално разположение. Един атом не може просто да има каквата и да е енергия: енергията която имат е строго определена от детайлната атомна структура. Когато електрон прескача от една орбита на друга, промяната кореспондира на точно определено количество енергия която се емитира под форма на фотон. Енергията на този фотон определя и цвета му.
Понеже много различни прескачания са възможни, всеки атом може да излъчи набор от различни цветове светлина. Ако тази светлина се разцепи от призма или дифракционна решетка, всеки цвят е видим като емисионна линия в спектъра, самия който се нарича линеарен спектър.
За да се демонстрира формирането на емисионна линия, да погледнем какво се случва когато обикновенна трапезна сол (Натриев Хлорид NaCl) се сложи в пламъка на свещ. Горната снимка показва непрекъснатия спектър на пламъка, точно както при лампата с нагорещена жичка. Когата щипка сол се постави на върха на ножа в пламъка на свеща, слаба оранжева линия се появява в спектъра, което кореспондира на емисионната линия на Натрия (Na, с 589нм).
Атомът не само излъчва светлина, но също така поглъща протони със същата енергия. Ако светлина премине през студен ниско-енергиен газ, атомите абсорбират специфични честоти причинявайки тъмните линии в спектъра, които се наричат абсорбционни линии.
Снимка от Марк Тиеле Вестра
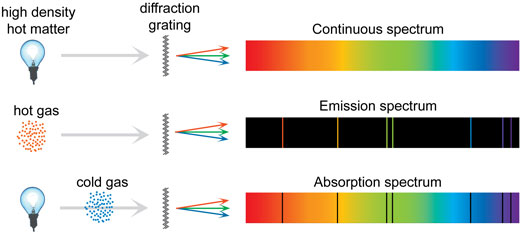
Но ако всички спектри се формират от атоми излъчващи рязко дефинирани цветове, как тогава са формирани непрекъснатите спектри? За единствен атом, незасегнат от външни влияния, линиите са действително резки. Такъв е случая в газове с ниска плътност такива като във флуоресцентните тръби. Във газове в високо налягане, като например Слънцето, а също така в течности и твърди вещества, има чести колизии и други механизми които причиняват линиите да губят тази рязкост и изглеждат замъглени, което води до непрекъснат спектър. Трите типа спектри са обобщени в долната илюстрация
Различните атоми (и молекули) имат различни емисионни и абсорбционни спектри. Тази разлика може да бъде използвана: просто гледайки към светлината идваща от обект в далечината, например Слънцето или звезда, ние можем да кажем кои химични елементи присъстват. На Земята, тази техника може да се използва като се облъчва със светлина една проба (често газ) и се измерва абсорбционния спектър, от което пък може да се съди за композиционния състав на тази проба.
Соларния спектър
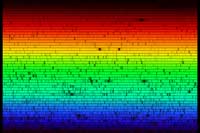
Ако изнесем нашия спектромер навън, ние можем да видим спектъра на слънчевата светлина. Спектъра показан по-долу, изглежда непрекъснат на пръв поглед. Но ако погледнем от близо, няколко тъмни линии могат да бъдат идентифинирани, които са предизвикани от абсорбирането на специфични честоти от атомите във външните слоеве на Слънцето, и на Земната атмосфера. Снимката по-долу не е много ласкателна за възможностите на нашия спектрометър: с просто око абсорбционните линии могат да се видят по-детайлно.
Абсорбционните линии които наблюдаваме в соларния спектър имат име:Фрауенхофер линии. Джозеф фон Фраунхофер (1787-1826) е първият който систематично изучава и измерва тези тъмни линии, въпреки че той не е първият който ги е наблюдавал. Всичко на всичко той е регистрирал 570 линии, които е категоризирал и наименовал.

Снимка на Марк Тиеле Вестра
Около 1860, Киркхоф и Бунзен откриват че всеки химически елемент е ассоцииран с комплект от спектрални линии. Те заключават че линиите на Фраунхофер в соларния спектър са причинени от абсорбирането на специфични цветове на светлината във външните слоеве на Слънцето. Някои от линиите са също така причинени от абсорбирането на светлина от атоми в атмосферата на Земята, като Кислород. Изучаването на тези линии накрая доведе до откритието на елемента Хелий на Слънцето, което пък е доказателство че Слънцето е захранвано от термоядрени процеси. Файл:
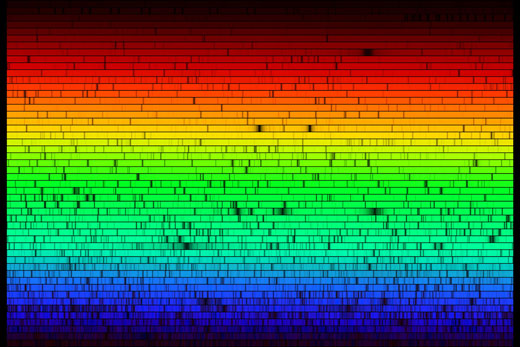
Снимка на National Optical Astronomy Observatory/Association of Universities for Research in Astronomy/National Science Foundation
С помощта на…
Авторът е изключително благодарен на Ксиаожин Жу от Университета Винсконсин-Мадисън, който предостави много от идеите и за конструкцията на спектрометъра (www.cs.cmu.edu/~zhuxj/astro/html/spectrometer.html) и на неговата страница можете да видите различни видове спректра. Благодарности също и на Бартян цан дер Меер, който ми подсказа за този фантастичен проект.
Resources
- Уикипедия дефиниция на видимия спектър
General info on spectra
- Уикипедия статия за електромагнетичния спектър
- Уикипедия статия за спектроскопа
- Уикипедия статия за Фраунхофер линии
Review
Марк Тиеле Вестра описва интересен и лесен експеримент за класната стая. Спектрометърът може да се конструира от налични и отпадъчни материали, и успешно демострира съставките на бялата светлина. Което е по-интересно е, че експериментът демострира как светлината може да се използва от астрономите да догатнат съставките на нашата близка звезда, Слънцето, както и на далечни звезди на слетлинни години от нас.
Експериментът демострира връзката между химията и физиката и може да е от полза за ученици от средно и висше образование.
Гетано Бугея, Малта





