Bursztyn: wprowadzenie do chemii organicznej Teach article
Tłumaczenie Marta Tondera. Czy wiedzieliście, że nazwy elektron i elektryczność pochodzą od bursztynu, „złota Bałtyku”? Wykorzystując w swoim cyklu lekcji skamieniałą żywicę Bernhard Sturm opowiada o przewodnictwie oraz innych właściwościach stałych substancji…
Wstęp

Zdjęcie dzięki uprzejmości
Steev Selby; źródło zdjęcia:
Wikimedia Commons
Bursztyn jest wykorzystywany do wyrobu biżuterii, jako składnik perfum oraz w medycynie ludowej od tysięcy lat. Oprócz tego znalazł swoje miejsce w nauce. Był pierwszą substancją u której grecki filozof Tales z Miletu (VI w p.n.e.) zaobserwował zjawisko elektrostatyczne, dzięki czemu bursztyn dał nazwę elektryczności: w 1601 roku angielski fizyk William Gilbert, który jako pierwszy rozróżnił przyciąganie magnetyczne i elektryczne, przypisał nazwę „electricus” właściwości przyciągania małych obiektów po potarciu, wywodząc to słowo od greckiej nazwy bursztynu – elektron, oznaczającej “błyszczący”.
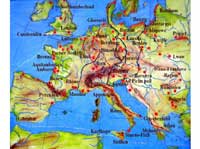
Miejsca odkrycia bursztynu
są oznaczone na czerwono,
historyczne szlaki
bursztynowe na czarno i
czerwono, a rzeki na
niebiesko. Kliknij na obrazek
aby powiększyć
Zdjęcie dzięki uprzejmości
Johannes Richter; źródło
zdjęcia: Wikimedia Commons
Bursztyn to żywica, która skamieniała wewnątrz rośliny lub już po wycieknięciu na wierzch. Kawałki bursztynu mogą mieć od 20 do 320 milionów lat, ale trudno być tego pewnym: datowanie radiowęglowe może być zastosowane wyłącznie przy okazach nie starszych niż 50 000 lat. Aby oszacować wiek bursztynu trzeba określić okres powstania otaczającego go osadu, chociaż bywa to zwodnicze, ponieważ bursztyn mógł powstać w innym miejscu niż to, w którym został znaleziony. Pomimo, że bursztyny są znajdowane na całym świecie, włączając w to Dominikanę, gdzie wydobywany jest rzadki niebieski bursztyn, prawdopodobnie najbardziej znane złoża znajdują się w Morzu Bałtyckim skąd pozyskiwane są ogromne ilości bursztynu. Można go także znaleźć w Europie Wschodniej, w rejonie Morza Północnego, w Alpach, północnej Hiszpanii i Sycylii. Kawałki bursztynu porwane z dna morza są wyrzucane przez fale, a ludzie zbierają je nurkując lub wygrzebując z piasku. W innych miejscach bursztyn jest wykopywany zarówno w kopalniach odkrywkowych jak i głębinowych.
Ta heterogeniczna, żółta do czerwonej organiczna makrocząsteczka krystalizuje się z dwóch rodzajów miękkiej, kleistej żywicy roślinnej: żywicy terpenoidowej lub fenolowej. Żywica terpenoidowa, produkowana zarówno przez rośliny okryto- jak i nagonasienne, składa się z pierścieni utworzonych z izoprenu (C5H8) Żywica fenolowa występuje wyłącznie w roślinach okrytonasiennych. Do grupy fenolowej zaliczamy m.in. ligninę, flawonoidy oraz niektóre barwniki.

Dominikany mający 25-40
milionów lat
Własność publiczna; źródło
zdjęcia: Wikimedia Commons
Żywica chroni uszkodzoną roślinę. Gdy wypływa na wierzch i twardnieje służy jako tarcza przeciw grzybom i owadom. Lotne drobinki żywicy pięknie pachną (przypomnijcie sobie zapach sosnowej żywicy), ale to kleiste, nielotne di-(C20) i triterpenoidy (C30) twardnieją i tworzą bursztyny poprzez polimeryzację rodnikową. Podczas procesu dojrzewania, który odbywa się na przestrzeni milionów lat, może dojść do polimeryzacji, izomeryzacji, sieciowania i cyklizacji, w efekcie dając mieszaninę cząsteczek o ogólnym wzorze C10H16O. Może się tam również znaleźć niewielka ilość siarki (do 1%).
Ponieważ bursztyn ma wiele typowych właściwości organicznego ciała stałego, takich jak uleganie spalaniu, nieprzewodzenie elektryczności i podatność na naładowanie elektrostatyczne, jest dobrym modelem do zaprezentowania tego rodzaju związków, pomimo jego zróżnicowanej i skomplikowanej kompozycji. Dodatkową wartością jest możliwość przedstawienia chemii w szerszym kontekście, ponieważ można nawiązać również do sztuki, biologii, nauk o Ziemi i fizyki. Umożliwia to dotarcie do uczniów którzy normalnie nie są zainteresowani przedmiotem.
Ten temat został opracowany na pięć godzin lekcyjnych dla uczniów w wieku 16+, którzy znają już pojęcia gęstości, przewodnictwa i obwodów elektrycznych. Nauczyciele mogą użyć podręczników z poprzednich klas, aby uczniowie odświeżyli swoją wiedzę. Cały cykl jest podzielony na sześć głównych zadań; w czasie czterech 45-minutowych lekcji grupy uczniów przechodzą do kolejnych stanowisk tak, żeby każda grupa wzięła udział raz w każdym zadaniu. Każde z tych zadań trwa około 20 minut. Dla dużej klasy mogą być potrzebne po dwa stanowiska na każde doświadczenie. Na ostatniej lekcji uczniowie będą prezentowali swoje wyniki przed klasą.

dzieci takie jak ten świetnie
się nadają do
eksperymentów.
Zdjęcie dzięki uprzejmości
Bernhard Sturm
Możliwe jest rozszerzenie opisanych zajęć o dodatkowe zadania (patrz niżej). Do niektórych dodatkowych działań może być potrzebna pomoc nauczycieli innych przedmiotów. Eksperymenty mogą zostać również przeprowadzone jako demonstracja przed klasą lub być robione równocześnie przez wszystkich uczniów. Metody zastosowane w zajęciach mogą być dosyć zróżnicowane, a ich wyniki powinny być łatwe do zapamiętania dla uczniów.
Bursztyn potrzebny do zajęć może zostać zakupiony w sklepach internetowych. 30-35 centymetrowy łańcuszek dla ząbkujących dzieci kosztujący od 8 do 20 euro (ok. 32 do 80 zł) jest wystarczający dla grupy około 30 uczniów. Uczniowie mogą również przynieść biżuterię z domu. Jedyny eksperyment w którym bursztyn zostanie zużyty i zniszczony to spalanie.
Podstawowe zadania
Dla najsprawniejszych uczniów można przygotować inne związki organiczne na których będą mogli przeprowadzić te same eksperymenty dla porównania z bursztynem. Mogą to być: do eksperymentu drugiego różne nasycone związki organiczne takie jak alkany np. gaz w palniku gazowym (z żółtym płomieniem) i zapalniczkę; do eksperymentów 3 i 6 plastik (np. polichlorek winylu lub polietylen) oraz różne rodzaje drewna (np. sosnę i dąb) i kalafonia (używana do smarowania smyczków skrzypcowych).
1) Pochodzenie geologiczne
Uczniowie mają za zadanie porównać datę i proces powstawania naturalnych złóż bursztynu, ropy naftowej i węgla, przy pomocy wiadomości znalezionych w Internecie i książkach. Powinni przy tym ocenić wiarygodność różnych źródeł informacji i zapisać daty i procesy znalezione w różnych miejscach. Dla stron internetowych powinni zanotować kiedy znaleźli te dane. W Tabeli 1możesz zobaczyć przykłady znalezionych danych.
| Źródła informacji | |||
|---|---|---|---|
| dtv-Lexikon, Munich, 1966 | http://en.wikipedia.org dnia31/03/2011 | ||
| Ropa Naftowa | Okres powstania | Okres kredy, 145-65 milionów lat temu | Milion lat temu |
| Powstawanie | Małe organizmy opadały na dno morza tworząc sapropel (organiczny muł). Zostały połączone w osad pod wpływem warunków beztlenowych i wysokiego ciśnienia. | Ogromne ilości prehistorycznego zooplanktonu i wodorostów osiadły na dnie zbiorników wodnych, gdzie panowały beztlenowe warunki. Materia organiczna została zmieszana z błotem i pogrzebana pod osadami. Ciepło i ciśnienie doprowadziły do powstania ropy naftowej. | |
| Węgiel | Okres powstania | Karbon, 360-300 milionów lat temu | Karbon (359-299 milionów lat temu) |
| Powstawanie | Szczątki obumarłych roślin osiadły na mule, a następnie zostały przykryte piachem i gliną. Wysokie ciśnienie i beztlenowe warunki doprowadziły do uwęglenia (karbonizacji). | Warstwy materiału roślinnego ułożyły się na spodzie zbiornika wody; błoto i woda o odczynie kwaśnym zapobiegły ich biodegradacji i utlenianiu. Zostały przykryte osadami i przeobrażone w węgiel. | |
| Bursztyn | Okres powstania | Od dewonu do trzeciorzędu, 400-40 milionów lat temu | Wyższy karbon (320 milionów lat temu) i później |
| Powstawanie | Żywica wyciekła z drzew na ziemię, przedostała się poniżej poziomu morza po zmianie klimatu i uległa polimeryzacji w beztlenowych warunkach. | Żywica, która znajdowała się w roślinach lub wypłynęła i dostała się do ziemi, często zabierała ze sobą zanieczyszczenia. Wysokie temperatury i ciśnienie wywołane przez nakładające się warstwy doprowadziły do powstania kopalu (stan przejściowy polimeryzacji i utwardzania, między gumowatą żywicą a bursztynem). Utrzymane wysokie temperatury i ciśnienie spowodowały oddzielenie się terpen, czego wynikiem było powstanie bursztynu. | |
2) Spalanie
Przypomnij swoim uczniom, że z powodu dużej zawartości węgla substancje organiczne kopcą przy spalaniu. Każdy uczeń powinien trzymać kawałek bursztynu (niem. Bernstein = Börnsteen – płonący kamień) w szczypcach nad probówką, a następnie podpalić bursztyn zapałką i obserwować popiół zbierający się w probówce.
Aby połączyć to doświadczenie z tematem zanieczyszczania powietrza przez spalanie w silnikach, uczniowie mogą zmieniać warunki spalania poprzez regulowanie płomienia w palniku Bunsena i przedyskutować jak można zapobiec powstawaniu sadzy.
Uwagi na temat bezpieczeństwa
Należy nosić okulary ochronne oraz uważać, aby nie przegrzać szklanej probówki, która może wybuchnąć. Nie wolno palić polichlorku winylu (jeden z materiałów do eksperymentów 3-6), ponieważ spowodowałoby to wydzielanie się szkodliwych związków. Zobacz równie ogólne informacje na temat bezpieczeństwa Science in School.

Zdjęcia dzięki uprzejmości Bernharda Sturma
3) Gęstość

krzemień (na wadze) mogą
zostać rozróżnione przez
stwierdzenie ich gęstości.
Kliknij na obrazek aby
powiększyć
Zdjęcie dzięki uprzejmości
Bernhard Sturm
Uczniowie określają gęstość bursztynu (1,050-1,096 g/ml), która jest tylko trochę wyższa niż wody (ok. 0,998 g/ml w temperaturze pokojowej). W tym doświadczeniu dokładniejsze wyniki można uzyskać używając większego kawałka bursztynu bez żadnych dziur. Sam lubię używać do porównania na lekcji dużego kawałka bursztynu i podobnego rozmiarami krzemienia, które posiadam, a uczniowie sami muszą rozpoznać je mierząc ich gęstość.
Potrzebne przybory: kawałek bursztynu, cylinder miarowy, woda (z kropelką płynu do zmywania dla zmniejszenia napięcia powierzchniowego i poprawy dokładności pomiarów) i waga.
Zważ bursztyn. Częściowo wypełnij cylinder wodą i zapisz objętość. Włóż bursztyn i zanotuj różnicę w objętości. Oblicz gęstość bursztynu ze wzoru:
Gęstość bursztynu [g/ml] = masa bursztynu [g]/objętość z bursztynem [ml]-objętość bez bursztynu[ml]
Wiele związków organicznych ma gęstość podobną do wody (0,8-1,2 g/ml). Polichlorek winylu, z gęstością 1,4 g/ml, jest nietypowy, w związku z jego cięższymi atomami chloru.
4) Oddzielanie bursztynu od mieszaniny substancji organicznych i nieorganicznych
Uczniowie nauczą się jak oddzielić bursztyn od kamieni i piasku. Jest to doświadczenie odnoszące się do czynności wykonywanych w kopalniach bursztynu.
- Zważ pustą zlewkę.
- Dodaj określoną objętość i ponownie zważ zlewkę, aby określić masę wody.
- Następnie dodaj mieszaninę piasku, kamieni i bursztynu i ponownie zważ zlewkę. Zanotuj również objętość.
- Stopniowo dodawaj sól i mieszaj dopóki bursztyn nie wypłynie. Ponownie zważ zlewkę i zanotuj objętość.
Jaka jest gęstość słonej wody? Użyj wzoru:
Gęstość słonej wody [g/l] = [(końcowa masa zlewki(4) – masa zlewki przed dodaniem soli(3)) + (masa zlewki z wodą(2) – masa pustej zlewki(1))] / [objętość wody + [końcowa objętość mieszaniny(4) – objętość wody bez soli(3))]
Wynik powinien być większy (>1,1 g/ml) niż gęstość bursztynu wyliczona w doświadczeniu 3, inaczej bursztyn nie wypłynąłby na wierzch.
Uczniowie mogą opisać swoje pomysły na rozwinięcie tej metody w technologię, która mogłaby być używana przy wydobywaniu bursztynu w kopalniach (zobacz zdjęcie poniżej).
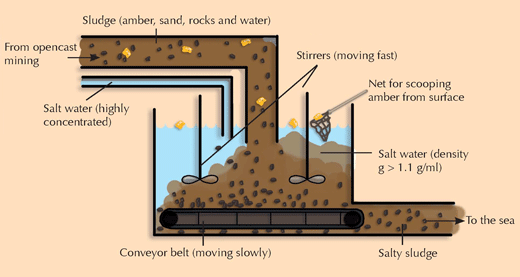
Zdjęcie dzięki uprzejmości Bernhard Sturm and Nicola Graf
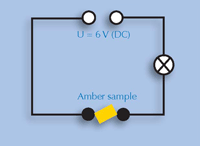
Bernhard Sturm
5) Przewodnictwo
Uczniowie dowiedzą się, że organiczne związki w formie stałej nie przewodzą elektryczności, poprzez zbudowanie obwodu elektrycznego z zasilacza, trzech kabli i żarówki służącego do sprawdzenia przewodnictwa bursztynu. Jeśli uczniowie nie wiedzą jak skonstruować ten obwód, mogą użyć podręczników do fizyki.
6) Separacja ładunków
Uczniowie poznają zjawisko indukcji elektrostatycznej i separacji ładunków przez wykonanie doświadczenia elektrostatycznego Gilberta: należy potrzeć bursztyn kawałkiem wełny i sprawdzić czy przyciąga małe kawałki papieru lub kawałki wysuszonego rdzenia czarnego bzu (Sambucus). Do tego doświadczenia świetnie nadają się małe bursztyny z naszyjników dla niemowląt.
Eksperyment nie wyjdzie przy dużej wilgotności powietrza, ponieważ woda, która przewodzi elektryczność zmniejszy ładunek elektrostatyczny na bursztynie. To samo spowodują mokre palce: dla lepszych efektów uczniowie mogą użyć izolowanej (plastikowej) pęsety aby przytrzymać bursztyn.

Zdjęcie dzięki uprzejmości V
Girard / D Néraudeau, UMR
CNRS 6118
Zadania opcjonalne
Robienie biżuterii
Aby połączyć sztukę z chemią i rozwinąć u uczniów umiejętności manualne, możesz zachęcić ich do zrobienia własnej biżuterii. Potrzebne będą nieobrobione kawałki bursztynu o średnicy co najmniej 15 mm. Każdy kawałek należy oszlifować wilgotnym papierem ściernym (grubość 120-1000) i wypolerować pastą do zębów. Następnie wypłukać w wodzie, wyczyścić ręcznikiem kuchennym i wetrzeć trochę oleju spożywczego przy pomocy ściereczki. Bursztyn przekłuć gorącą igłą (to powinien zrobić nauczyciel) lub wydrążyć 1-2 mm dziurkę. Nawlecz koralik na nitkę lub rzemyk aby zrobić bransoletkę lub naszyjnik.
Połączenia z biologią
Szukając połączeń z biologią, można pokazać uczniom inkluzje w bursztynach i szerzej omówić żywicę – jej skład, gdzie występuje, jaka jest jej funkcja i jaka jest struktura drewna.
Klasyfikacja bursztynów
Żywice roślinne są tak zróżnicowane, że po składzie chemicznym można określić z jakiego gatunku rośliny pochodzi konkretny bursztyn. Nie znaczy to, że żywica o podobnym składzie pochodzi z podobnym roślin: niedawne badania wykazały, że żywice z bardzo podobnym składem chemicznym mogą być wytworzone przez zupełnie nie spokrewnione rośliny (Bray & Anderson, 2009). Na podstawie składu chemicznego rozróżnia się pięć klas bursztynów:
- Klasa I: najczęściej występujące, składają się z kwasów labdanokarboksylowych; dzielą się na trzy podklasy
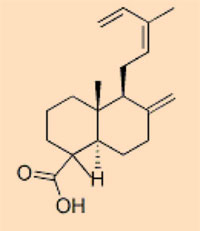
- Klasa II: powstałe z żywicy z podstawą seskwiterpenoidową, taką jak kadinen.
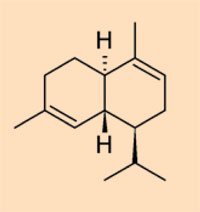
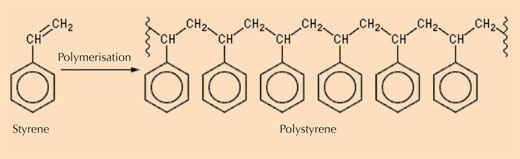
- Klasa III: naturalne polistyreny
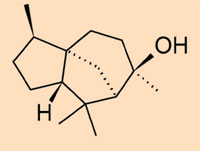
- Klasa IV: zbiór niespolimeryzowanych bursztynów, które zawierają głównie oparte na cedrenie seskwiterpenoidy.
- Klasa V: zazwyczaj produkowana przez sosny lub drzewa pokrewne; mieszanina żywicy diterpenoidowej i cząsteczek n-alkilowych (R-NH-CH3)
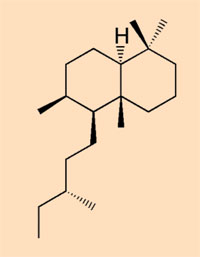
Własność publiczna; źródło zdjęcia: Wikimedia Commons; dostosowane przez Nicola
Badania nad bursztynem w ESRF

Fragmenty bursztynu są bogatym źródłem skamieniałości. W Europejskim Ośrodku Synchrotronu Atomowego (ESRF)w1w Grenoble we Francji potężne maszyny rentgenowskie są używane do badań nad inkluzjami w bursztynach. Jest to specjalnie przydatne przy nieprzezroczystych bursztynach, które są nie do zbadania dla paleontologów dysponujących klasycznymi mikroskopami. Tą techniką zostało zidentyfikowanych kilkaset inkluzji zwierząt z okresu środkowej kredy, sprzed 100 milionów lat.
W innym badaniu w ESRF naukowcy użyli tej samej techniki, aby otrzymać dokładny, trójwymiarowy obraz piór zatopionych w półprzezroczystym bursztynie, które mogły należeć do upierzonego dinozaura – stanu pośredniego w ewolucji współczesnych ptaków.
Aby uzyskać więcej informacji, przeczytaj w Internecie raportw2z ESRF, jednego z członków EIROforum, wydawcy Science in School.
References
- Bray PS, Anderson KB (2009) Identification of carboniferous (320 million years old) class Ic amber. Science 326(5949): 132-134. doi: 10.1126/science.1177539
-
Darmowy, pełny tekst artykułu dostępny na: www.sciencemag.org/content/326/5949/132.short
-
- Aby zobaczyć inne zajęcia z chemii i fizyki nadające nowego wymiaru lekcjom, na przykład polimeryzację rodnikową etenu do polietylenu, wejdź na:
-
Sturm B (2009) The drama of science. Science in School 13: 29-33.
-
Web References
- w1 – Więcej informacji o ESRF na: www.esrf.eu
- w2 – Informacje o naukowcach z ESRF, którzy użyli promieni rentgenowskich aby zobaczyć inkluzje: www.esrf.eu/news/general/amber
Resources
-
Aby pobrać wykresy z historią Ziemi, zobacz: www.stratigraphy.org/upload/ISChart2009.pdf or www.chronos.org/downloads/timetowerparis_highres.png
-
Aby dowiedzieć się więcej o badaniach nad plastikami biodegradowalnymi, zobacz:
-
Bradley D (2007) Plastics, naturally. Science in School 5: 66-69.
-
Institutions
Review
Bernhard Sturm, który opublikował już inny świetny artykuł w Science in School (Sturm, 2009), jest sztandarowym przykładem kreatywności na polu nauczania nauk ścisłych.
Wszyscy, którzy uważają, że chemia i fizyka są nudne powinni spróbować zajęć z bursztynem zaproponowanych przez autora. Zaczynając od tego starożytnego materiału i podążając za sugerowanymi rozszerzeniami nauczyciel będzie miał możliwość rozwinięcia różnych tematów związanych z bursztynem i ukazać nieoczekiwane powiązania ze sztuką i naukami humanistycznymi.
Kolejne doświadczenia pozwalają na poznanie chemii organicznej (naturalne i sztuczne polimery), nauk o Ziemi (skały osadowe, skamieniałości, paliwa kopalniane), fizyki (gęstość, metody oddzielania, przewodnictwo i separacja ładunku), nauki o środowisku (spalanie, zanieczyszczenie) i biologii (żywica, inkluzje w bursztynie).
Dla zainteresowanych w połączeniach z innymi dziedzinami wybór także jest szeroki: sztuka i rzemiosło (robienie biżuterii), historia (Szlak Bursztynowy, Komnata Bursztynowa) czy ekonomia (wydobywanie i sprzedawanie bursztynu) oraz wiele innych.
Jedyne, czego potrzebuje nauczyciel do podążania za Bernhardem Sturmem ścieżkami Talesa z Miletu, Williama Gilberta i innych, to kawałki “złota Bałtyku” (na szczęście dużo tańszego niż prawdziwe złoto).
Ten artykuł może być przydatny jako wprowadzenie przed wizytą w muzeum historii naturalnej lub nauki i może być także użyty jako ćwiczenie na czytanie ze zrozumieniem. Przykładowe pytania dotyczącego przeczytanego tekstu:
- Aby określić wiek fragmentu bursztynu:
- można normalnie użyć datowania radiowęglowego
- trzeba określić wiek otaczających go osadów
- wybiera się metodę odpowiednią do okoliczności
- Który z następujących materiałów najbardziej różni się gęstością od bursztynu?
- polietylen
- polichlorek winylu
- drewno dębowe
- kalafonia
Giulia Realdon, Włochy

