Natuurlijke selectie op moleculair niveau Understand article
Vertaald door Pascal te Welscher. Het is bekend dat bepaalde genetische sequenties ons kunnen helpen te overleven in ons milieu - dit is de basis van evolutie. Het is echter niet eenvoudig om aan te tonen welke genetische sequenties gunstig zijn en hoe zij ons helpen te overleven – vooral niet…

iStockphoto
Toen mensen 150.000 jaar geleden voor het eerst Afrika verlieten en zich vestigden in de valleien van de Tigris en de Eufraat, zeilden tussen de eilanden van Indonesië en de Beringstraat overstaken, werden zij met veel uitdagingen geconfronteerd. Komende uit de hete, droge savannes van Afrika moesten de eerste populaties zich aanpassen aan de lokale klimaatsfactoren en veranderden over vele generaties hun uiterlijk en fysiologie (Harris & Meyer, 2008). Zo werd bijvoorbeeld de huid van mensen die leefden in minder zonnige streken steeds bleker (Lamason et al., 2005) en binnen populaties waarin mensen melk dronken van gedomesticeerde dieren behielden uiteindelijk ook volwassenen de mogelijkheid om lactose te verteren terwijl deze eigenschap normaal snel verloren gaat na de kindertijd (Tishkoff et al., 2007). Populaties die zetmeelrijk voedsel aten produceerden in de loop der tijd meer amylase in het speeksel dat helpt om zetmeel af te breken (Perry et al., 2007).
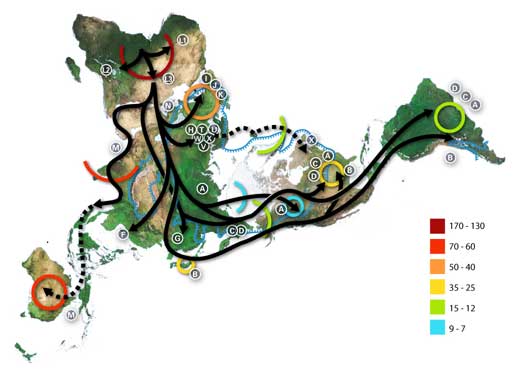
Getallen geven het aantal duizenden jaren geleden aan.
De blauwe lijn duidt het gebied dat gedurende de laatste grote ijstijd overdekt was met ijs of toendra. De letters op de pijlen geven groepen mensen aan die tot dezelfde mitochondriale haplogroep behoren; Haplogroepen kunnen worden gebruikt om genetische populaties te beschrijven en zijn als zodanig vaak geografisch van aard.
Bijvoorbeeld, de gebruikelijke indeling voor mtDNA haplogroepen wordt als volgt beschreven:
Afrikaans: L, L1, L2, L3, L3
Nabij Oosters: J, N
Zuid-Europees: J, K
Algemeen Europees: H, V
Noord-Europees: T, U, X
Aziatisch: A, B, C, D, E, F, G (let wel: M bestaat uit C, D, E en G)
Inheems Amerikaans: A, B, C, D, en soms X.
Klik op de afbeelding om te vergroten
Figuur met dank aan Avsa; bron: Wikimedia Commons
In ieder geval wordt van enkele van deze veranderingen veronderstelt dat zij het gevolg zijn van positieve selectie (zie verklarende woordenlijst voor alle cursieve termen). Dat betekent dat voor een specifiek milieu (de selectiedruk) in het verleden populaties waarbinnen individuen voorkwamen met een voordelige DNA sequentie een grotere overlevingskans hadden dan die populaties waarbinnen dergelijke sequenties niet voorhanden waren. Tegenwoordig kunnen wetenschappers met behulp van de genoomsequenties van vele soorten, inclusief mensen en hun naaste evolutionaire verwanten, eigenschappen en DNA sequenties van populaties of soorten met een verschillende levensstijl en uit een verschillend milieu met elkaar vergelijken. Dit stelt onderzoekers in staat om sequenties te identificeren die een rol gespeeld zouden kunnen hebben bij adaptaties en de functie en de aanpassingswaarde van een DNA sequentie voor een organisme te onderzoeken.

iStockphoto
De sequentievariaties van sommige genen die betrokken zijn bij het bepalen van de huidskleur bijvoorbeeld vertonen een specifiek geografisch patroon; sequentievergelijkingen tussen Europeanen en Afrikanen in het bijzonder suggereren dat variatie in de huidskleur het gevolg is van positieve selectie. Een lichte huidskleur correleert positief met de breedtegraad en er zijn verschillende hypothesen naar voren gebracht om de mogelijke voordelige effecten daarvan uit te leggen.
Eén hypothese baseert zich op de waarneming dat mensen met een donkere huidskleur op een hoge breedtegraad lijden aan vitamine D deficiëntie en stelt dat een lichte huidskleur gunstig is voor de productie van vitamine D. Mensen met een lichte huidskleur zijn daarentegen meer gevoelig voor de schadelijke effecten van zonlicht; meer blootstelling aan het zonlicht correleert met een toename in het aantal gevallen van huidkanker bij mensen met een lichte huidskleur. Een lichte huidskleur in menselijke populaties die leven op een hoge breedtegraad zou daarom een evolutionair compromis kunnen zijn tussen de afname in de bescherming tegen de kankerverwekkende effecten van zonlicht en de toename in de productie van een essentieel vitamine.
Ondanks dat het een aannemelijke hypothese is blijft de waarneming waarop de hypothese steunt echter een indirect bewijs. Om de aanpassingswaarde van deze eigenschap aan te tonen zou men moeten meten of dat individuen met een lichte huidskleur op een hoge breedtegraad een verhoogde kans op overleven en toegenomen reproductie vertonen.
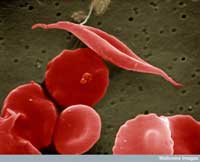
afbeelding van sikkelcel en
andere rode bloedcellen
Figuur met dank aan EM Unit,
UCL Medical School, Royal Free
Campus / Wellcome Images
Dergelijke experimenten met onze soort blijven echter moeilijk om te doen: overlevings experimenten (waarbij individuen met verschillende eigenschappen bloot gesteld moeten worden aan een specifiek milieu om te zien welke overleven) kunnen om ethische redenen niet worden uitgevoerd met mensen en onze lange generatietijd maakt het moeilijk om verschillen in reproductiesnelheid aan te tonen. De omstandigheden waarin het mogelijk is om de aanpassingswaarde van een menselijke eigenschap te bestuderen blijven daarom erg beperkt – maar ze bestaan wel.
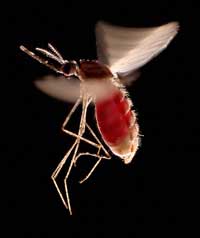
vol met bloed. Deze soort,
Anopheles stephensi, is de
insect vector die malaria
overbrengt in India en
Pakistan
Figuur met dank aan Hugh
Sturrock / Wellcome Images
Eén voorbeeld heeft betrekking op twee ziektes: sikkelcelanemie en malaria. Sikkelcelanemie is een erfelijke aandoening en van het gen bestaan twee varianten, oftewel allelen: het gangbare allel voor hemoglobine en het sikkelcel allel voor het zogenaamde hemoglobine S. Sikkelcelanemie is een recessieve ziekte en in het geval een persoon een enkel sikkelcel allel draagt komen er slechts onder bepaalde omstandigheden ziekteverschijnselen voor, terwijl mensen met twee sikkelcel allelen de serieuze symptomen vertonen die gepaard gaan met bloedarmoede. Sterftecijfers tonen echter aan dat het sikkelcel allel ook voordelig kan zijn voor een drager: in populaties die bloot staan aan de malaria parasiet hebben individuen met een enkel sikkelcel allel betere overlevingskansen omdat de malaria parasiet (Plasmodium falciparum) gezonde bloedcellen nodig heeft om de gastheer binnen te dringen en om zich te vermenigvuldigen. De frequentie van het sikkelcel allel neemt daarom toe in populaties die geteisterd worden door malaria – het allel is adaptief in dit specifieke milieu.
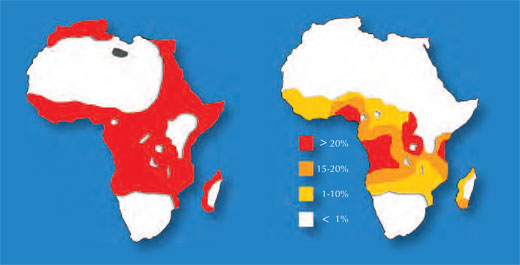
Figuur met dank aan Anthony Allison; bron: Wikimedia Commons
Een ander voorbeeld dat de aanpassingswaarde van een menselijke eigenschap aantoont heeft betrekking op een fragment van chromosoom 17 waarvan bekend is dat het meer dan drie miljoen jaar geleden een inversie – een chromosomale herschikking – heeft ondergaan in onze voorouders (Stefansson et al., 2005). Het feit dat deze inversie verspreid voorkomt binnen Europese populaties suggereert dat het positief is geselecteerd – het heeft een voordeel verleend aan de dragers. Om deze hypothese te testen hebben wetenschappers bijna 30.000 IJslanders gegenotypeerd en waren met die informatie in staat om aan te tonen dat over de laatste 80 jaar individuen met de inversie 3.2% meer nageslacht per generatie hebben geproduceerd ten opzichte van individuen zonder deze inversie. Dat levert een plausibele verklaring voor de snelle verspreiding van deze chromosomale herschikking.
Bovenstaande voorbeelden maken duidelijk dat positieve selectie zich recentelijk heeft voorgedaan in menselijke populaties, maar het is vaak onbekend waarom een bepaalde sequentievariant een selectief voordeel biedt. Om de oorzakelijke verbanden tussen mogelijk adaptieve DNA sequenties en de fitness van een individu op moleculair niveau te verklaren richten wetenschappers zich op organismen waarmee men eenvoudiger kan experimenteren dan met mensen.
Een goed voorbeeld betreft de schutkleur van de zogenaamde Oldfield muis, Peromyscus polionotus. Oldfield muizen die leven op het strand van Florida hebben een veel lichtere vacht dan de soortgenoten die meer landinwaarts leven. De aanpassingswaarde van deze eigenschap werd meer dan 30 jaar geleden aangetoond: muizen met een vacht waarvan de kleur overeen komt met de kleur van de bodem worden veel minder door uilen gegeten dan muizen die minder zijn gecamoufleerd. Wetenschappers hebben echter slechts recentelijk de genetische loci die verantwoordelijk zijn voor deze adaptieve eigenschap kunnen identificeren (Hoekstra et al., 2006): het blijkt dat variatie in de kleur van de vacht grotendeels afhankelijk is van het McR1 gen. Het eiwit waarvoor dit gen codeert werkt als een biochemische schakel tussen de productie van enerzijds eumelanine, een donker pigment in de huid, en anderzijds pheomelanine, een licht pigment. De verschillende allelen van het McR1gen activeren het reactiepad dat de aanmaak van pigment aanstuurt in meer of mindere mate met als gevolg dat de productie van het ene pigment dat van de ander overheerst.
vergroting van de
methicilline resistente
Staphylococcus aureus
bacterie
Figuur met dank aan Annie
Cavanagh / Wellcome Images
Een ander voorbeeld van een aangetoond oorzakelijk verband betreft Staphylococcus aureus, een bacterie die verschillende ziekten kan veroorzaken zoals longontsteking of ontsteking van de hartkleppen. In een experiment werd een patiënt met herhaalde S. aureus infecties voor drie maanden behandeld met vancomycine, één van de weinige antibiotica die nog steeds effectief zijn tegen S. aureus. Vooraf en met intervallen gedurende de behandeling werden door onderzoekers monsters afgenomen van het pathogeen en werd het gehele genoom van het eerste en laatste monster gesequenced. Toen de onderzoekers de drie miljoen basenparen (de ‘letters’ van de genetische code) van het bacteriële genoom bestudeerden bleek dat er slechts 35 verschillen bestonden tussen het eerste en het laatste monster.
Door de relevante DNA fragmenten van de tussenliggende monsters te sequencen kon de volgorde van de veranderingen over de tijd worden vastgesteld. Vervolgens werd in vitro de bacteriële resistentie van de verschillende monsters tegen vancomycine getest en op deze wijze konden specifieke genetische veranderingen worden gecorreleerd met de effecten van het medicijn op de bacteriële groei en respons. Tussen het eerste en tweede monster, bijvoorbeeld, hadden zes nucleotide substituties (veranderingen in de ‘letters’) plaatsgevonden in twee genen. Deze zes mutaties alleen al boden een voordeel; zij verviervoudigden de bacteriële tolerantie voor vancomycine met als gevolg dat deze bacteriën zich beter konden voortplantten en als zodanig de overhand kregen in het lichaam van de patiënt. Over de daarop volgende weken deden zich nog zesentwintig verdere mutaties voor die de tolerantie nog eens verdubbelden en effectief een vancomycine-tolerante lijn van S. aureus vormden (Mwangi et al., 2007).
In het kort komt het er op neer dat het onderzoek naar de moleculaire basis van adaptieve evolutie in wilde populaties niet eenvoudig is. Het definiëren van een selectiedruk, het identificeren van de DNA sequentie achter geassocieerde eigenschappen, het meten van de fitness van een individu en het uitwerken van een mechanistische verklaring voor de wijze waarop veranderingen in de DNA sequentie de adaptieve eigenschap beïnvloeden behoren alle tot de uitdagingen van deze wetenschap. Het gebruik van model dieren en nieuwe ontwikkelingen in de technologie maken dit soort onderzoek echter wel meer toegankelijk en vergroten als zodanig ons begrip over de relatie tussen veranderingen op genetisch niveau en de mogelijkheid van organismen om zich aan te passen aan hun leefomgeving.
Verklarende Woordenlijst
Aanpassingswaarde: een eigenschap heeft een aanpassingswaarde als deze het individu helpt beter te overleven en voort te planten in een bepaald milieu dan andere individuen van dezelfde soort die deze eigenschap niet bezitten. Een eigenschap wordt formeel als adaptief beschouwd wanneer het de fitness vergroot.
Allel: een variant van een gen.
Fitness: een moeilijk te definiëren formele term uit de evolutie biologie en de populatie genetica; Het beschrijft het gemiddeld aantal nakomelingen van een generatie met een bepaald genotype in vergelijking met dat van een ander genotype binnen een populatie. Genotypen met relatief meer nageslacht hebben dus een hogere fitness. Voor een goed overzicht van het begrip fitness en genotype, zie Wikipediaw1.
Genoom: één complete set van chromosomen van een organisme. Er wordt meestal vanuit gegaan dat hiermee het nucleair DNA wordt aangeduid in tegenstelling tot plastide of mitochondriaal DNA. Voor meer informatie, zie ‘What is a genome’ op de website van de US National Library of Medicinew2.
Positieve selectie: natuurlijke selectie is een mechanisme dat in de natuur evolutie veroorzaakt; Natuurlijke selectie houdt in dat organismen die beter in hun omgeving passen, meer kans hebben om te overleven en voor nakomelingen te zorgen dan minder goed aangepaste organismen. Natuurlijke selectie wordt ‘positief’ genoemd als het bepaalde eigenschappen van een individu bevoordeeld en het individu door die eigenschappen beter in staat is te overleven en steeds meer de overhand neemt in een populatie.
Selectiedruk; een aanduiding voor de effecten die de natuurlijke selectie uitoefent op de genetische variabiliteit binnen een bepaalde populatie. Een verschil aan eigenschappen tussen de individuen binnen een populatie kan door selectiedruk leiden tot een verschil in overlevingskansen.
Eigenschap: een enkel kenmerk of een set aan kenmerken dat een organisme karakteriseert (bijv. de lengte of de kleur van de vacht).
Met dank aan
De auteur is David Hughes, Mehmet Somel en Ania Lorenc dankbaar voor het becommentariëren van dit artikel.
References
- Harris EE, Meyer D (2006) The molecular signature of selection underlying human adaptations. American Journal of Physical Anthropology 131(S43): 89-130. doi: 10.1002/ajpa.20518
- Dit artikel geeft een goed overzicht van het onderzoek met betrekking tot de moleculaire evolutie van mensen.
- Hoekstra H et al. (2006) A single amino acid mutation contributes to adaptive beach mouse color pattern. Science 313: 101-104. doi: 10.1126/science.1126121
- Dit en andere artikelen van Hopi Hoekstra’s onderzoek team over de vachtkleur van muizen zijn verkrijgbaar op de website van Harvard University: www.oeb.harvard.edu/faculty/hoekstra/Links/PublicationsPage.html
- Zie ook het vervolg artikel waarin Agouti, de negatieve regulator van McR1, bij draagt aan de adaptieve vachtkleur in Peromyscus:
- Steiner CC, Weber JN, Hoekstra HE (2007) Adaptive variation in beach mice produced by two interacting pigmentation genes. PLoS Biology 5: e219. doi: 0.1371/journal.pbio.0050219
- Dit en andere artikelen in PLoS Biology zijn online gratis verkrijgbaar.
- Het volgende artikel bespreekt de adaptieve pigmentatie in gewervelde dieren:
- Hoekstra HE (2006) Genetics, development and evolution of adaptive pigmentation in vertebrates. Heredity 97: 222-234. doi: 10.1038/sj.hdy.6800861
- Dit artikel is gratis verkrijgbaar op de website van het tijdschrift Heredity: www.nature.com/hdy
- Een overzicht van Hopi Hoekstra’s laatste onderzoek is verkrijgbaar op John Hawks’ blog: http://johnhawks.net/weblog/topics/evolution/selection/hoekstra-2009-adaptive-pigmentation.html
- Lamason RL et al. (2005) SLC24A5, a putative cation exchanger, affects pigmentation in zebrafish and humans. Science 310: 1782-1786. doi: 10.1126/science.1116238
- Mwangi MM et al. (2007) Tracking the in vivo evolution of multidrug resistance in Staphylococcus aureus by whole-genome sequencing. Proceedings of the National Academy of Sciences of the United States of America 104: 9451-9456. doi: 10.1073/pnas.0609839104
- Perry GH et al. (2007) Diet and the evolution of human amylase gene copy number variation. Nature Genetics 39: 1256-1260. doi: 10.1038/ng2123
- Bekijk voor een overzicht van dit onderzoek ook de Panda’s Thumb: http://pandasthumb.org/archives/2008/12/amylase-and-hum.html
- Stefansson H et al. (2005) A common inversion under selection in Europeans. Nature Genetics 37: 129-137. doi: 10.1038/ng1508
- Bekijk voor een overzicht van het artikel Evolgenn: http://evolgen.blogspot.com/2005/02/human-inversion-under-selection.html
- Tishkoff SA et al. (2006) Convergent adaptation of human lactase persistence in Africa and Europe. Nature Genetics 39: 31-40. doi: 10.1038/ng1946
- Bekijk voor een overzicht van dit onderzoek ook The New York Times: www.nytimes.com/2006/12/10/science/10cnd-evolve.html?_r=1
Web References
- w1 – Voor een goed overzicht van de termen ‘fitness’ en ‘genotype’, zie Wikipedia: http://en.wikipedia.org/wiki/Fitness_(biology) en http://en.wikipedia.org/wiki/Genotype
- w2 – Voor meer informatie over genomen en het Human Genome Project, zie ‘What is a genome’ op de website van de US National Library of Medicine: http://ghr.nlm.nih.gov/handbook/hgp/genome
Resources
- Als je dit artikel interessant vond, dan zijn de volgende Science in School artikelen over evolutie mogelijk ook de moeite waard om te lezen:
- Haubold B (2010) Review of Why Evolution is True. Science in School 14. www.scienceinschool.org/2010/issue14/evotrue
- Leigh V (2008). Interview with Steve Jones: the threat of creationism. Science in School 9: 9-17. www.scienceinschool.org/2008/issue9/stevejones
- Patterson L (2010) Getting ahead in evolution. Science in School 14: 16-20. www.scienceinschool.org/2010/issue14/amphioxus
- Pongsophon P, Roadrangka V en Campbell A (2007) Counting Buttons: demonstrating the Hardy-Weinberg principle. Science in School 6: 30-35. www.scienceinschool.org/2007/issue6/hardyweinberg
- Voor meer informatie over malaria, zie:
- Hodge R (2006) Fighting malaria on a new front. Science in School 1: 72-75. www.scienceinschool.org/2006/issue1/malaria
- Om meer te weten te komen over de structuur van zetmeel dat door amylase wordt afgebroken, zie:
- Cornuéjols D (2010) Starch: a structural mystery. Science in School 14: 22-27. www.scienceinschool.org/2010/issue14/starch
Review
Dit artikel beschrijft een aantal interessante voorbeelden van evolutionaire adaptaties in mensen op moleculair niveau. De nadruk wordt gelegd op het probleem om causale verbanden te leggen tussen adaptieve DNA sequenties en de fitness van het individu, enerzijds, en het belang van dit onderzoek aan meerdere Het artikel biedt geschikt materiaal voor inzichtelijke vragen met betrekking tot de begrippen natuurlijke selectie en fitness in mensen en andere organismen. Bijvoorbeeld:
- Verklaar de processen die zijn betrokken bij natuurlijke selectie.
- Wat wordt er bedoeld met de term ‘fitness’?
- Verklaar waarom het sikkelcel allel een selectievoordeel heeft in menselijke populaties.
- Wat zijn de problemen met het vaststellen van causale verbanden tussen adaptieve DNA sequenties en fitness in mensen?
- Maak een stroomdiagram om de adaptieve waarde van de vachtkleur in Oldfield muizen te verklaren.
- Hoe was het voor wetenschappers mogelijk om de genetische veranderingen in Staphylococcus aureus te correleren met bacteriële groei en weerstand tegen antibiotica?
Dit artikel maakt het leerlingen ook mogelijk een verband te leggen tussen DNA, aminozuursequentie en eiwit structuur en functie in sikkelcelanemie. De tekst is geschikt om discussies in the klas te leiden die betrekking hebben op het onderzoek naar de moleculaire basis van evolutionaire verwantschappen en de ethica omtrend genetische testen binnen menselijke populaties.
Mary Brenan, VK
